このページでは、中学1年生で学習する再結晶について、中学生向けに解説をしていくよ。
 ねこ吉
ねこ吉よろしくお願いします!
うん。よろしくね!
このサイトが本になりました!
わかりやすい解説・画像・動画が1冊に!



中学生・大人の学び直し・理科の先生などにオススメ!
再結晶の学習に必要な用語
溶質・溶媒・溶液
再結晶の説明をする前に、再結晶の学習をするために必要な用語を確認しておこう。



再結晶を学習するのに必要な用語?
うん。大切なのは次の3つだよ。
- 溶質 ⋯ 液体に溶けている物質のこと
- 溶媒 ⋯ 物質が溶けている液体のこと
- 溶液 ⋯ 溶質と溶媒を合わせたもの
表にすると以下のようになるね。
| 溶質 | 溶媒 | 溶液 |
  |   |   |
| 砂糖 食塩 など | 水 エタノール など | 食塩水 砂糖水 など |



溶質と溶媒を合わせたものが溶液なんだね!
そういうことだね。
まずはこれらの用語をしっかりと覚えておこう!
溶解度
次は溶解度という言葉の意味をしっかりと理解しよう
溶解度とは「水100gに溶かすことができる限界の量」のことだよ!
溶解度 ⋯ 水100gに溶かすことができる限界の量
例えば、40℃の水が100gあったとするね。
この水に、ミョウバンを少しずつ溶かしていこう。
このとき、ミョウバンを24g溶かしたら、それ以上は溶けなくなるんだ。(水の中にミョウバンの粒が残ってしまう)
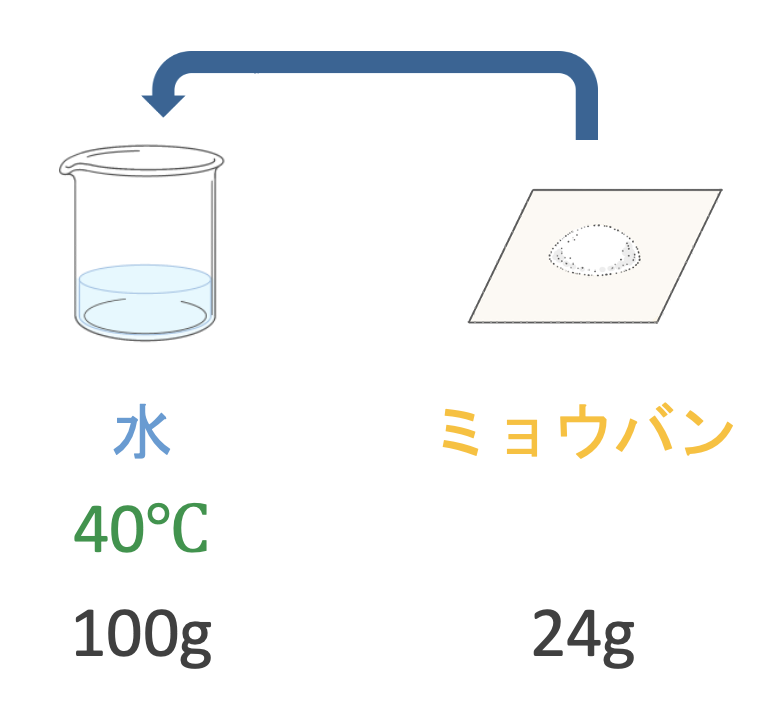

つまりミョウバンが、40℃の水100gに溶ける限界は24gだよね。
このとき、溶解度24(g)というんだよ!



なるほどね!
溶解度について詳しく知りたい人は、こちらのページを読んでから、またこのページに戻ってきてね。
再結晶とは
では、再結晶について学習をしていこう。
再結晶とは「液体に溶けた物質を、再び結晶としてとりだすこと」なんだ。
再結晶 ⋯ 液体に溶けた物質を、再び結晶としてとりだすこと



なんだか難しい⋯。
例をもとに説明していくね。
下のグラフを見てみよう。これはミョウバンの溶解度を示した溶解度曲線だね。
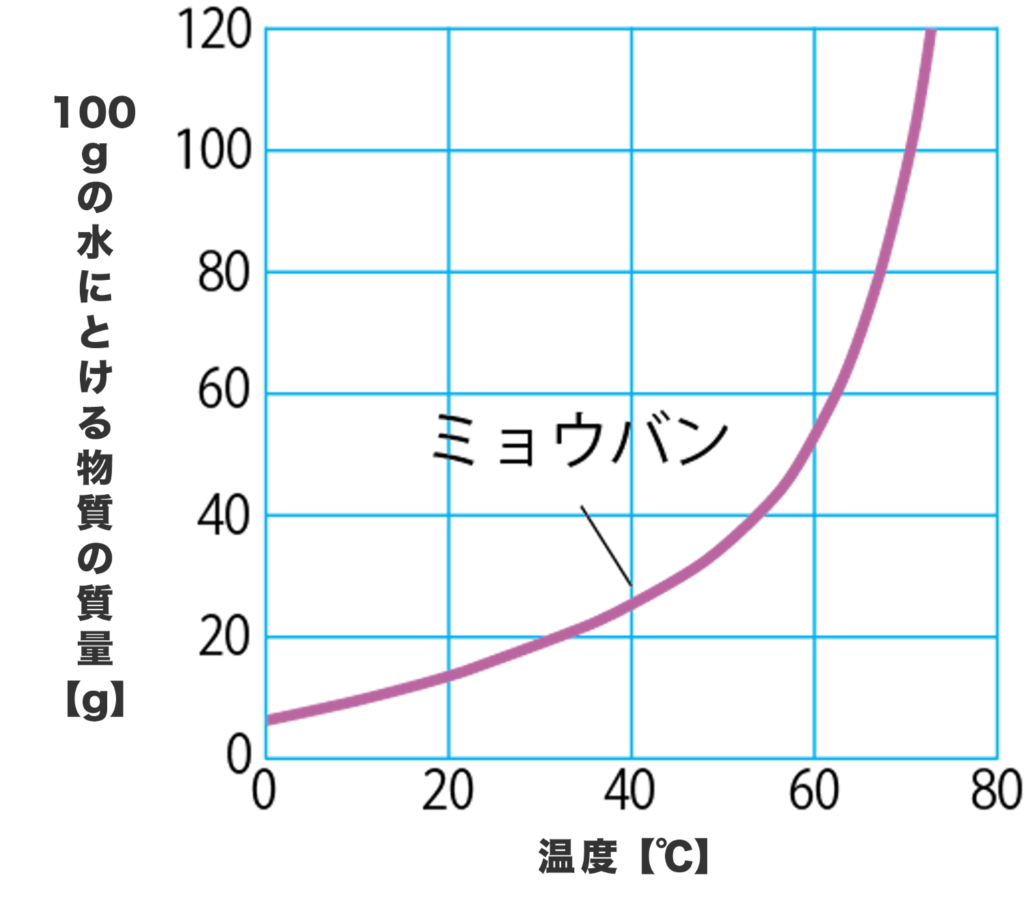

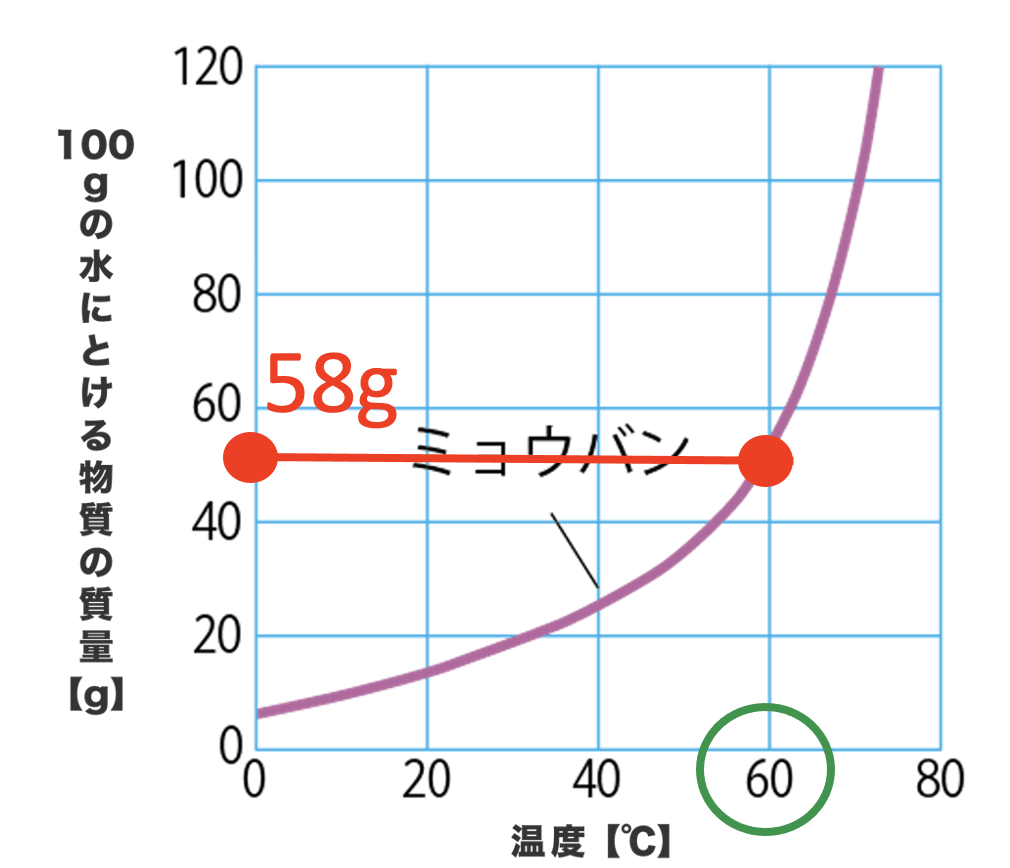
さて、ねこ吉。60℃の水100gがあったとき、この水にミョウバンは何gまで溶けることができるかわかるかな?



グラフを見ると⋯。(約)58gだね!
その通り!水の温度(横軸)が60℃だから、溶けるミョウバンの量(縦軸)は58gだね。

さて、ねこ吉。この、一度水に溶かしてしまったミョウバン、どうすれば再び結晶として取り出すことができるかわかるかな?



一度溶けたものを取り出す?そんなことができるの?
できるんだ。それが再結晶という方法だよ。
方法は簡単。水溶液の温度を下げればいいんだ。
ここでは60℃から20℃まで水の温度を下げてみよう。
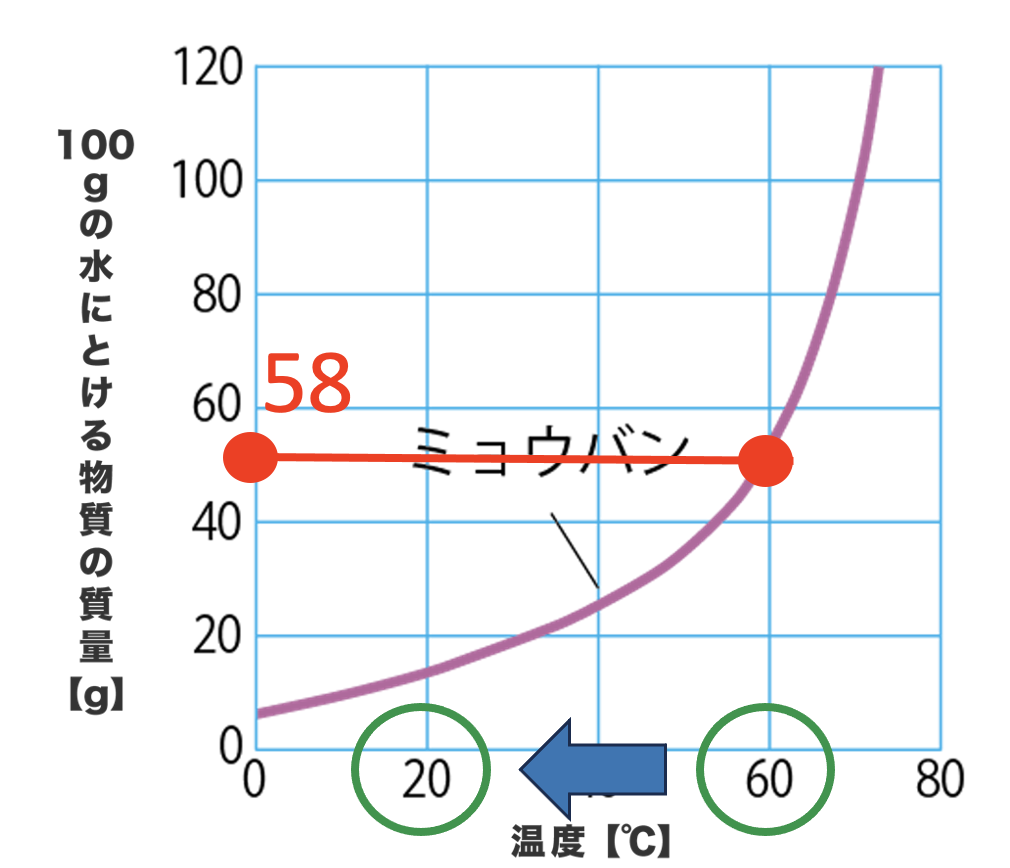




温度を下げるとどうなるの?
溶解度は温度によって変化したよね。
60℃のときは、ミョウバンが58gまで溶けることができたけれど、20℃になると、ミョウバンが11gまでしかとけることができないね。
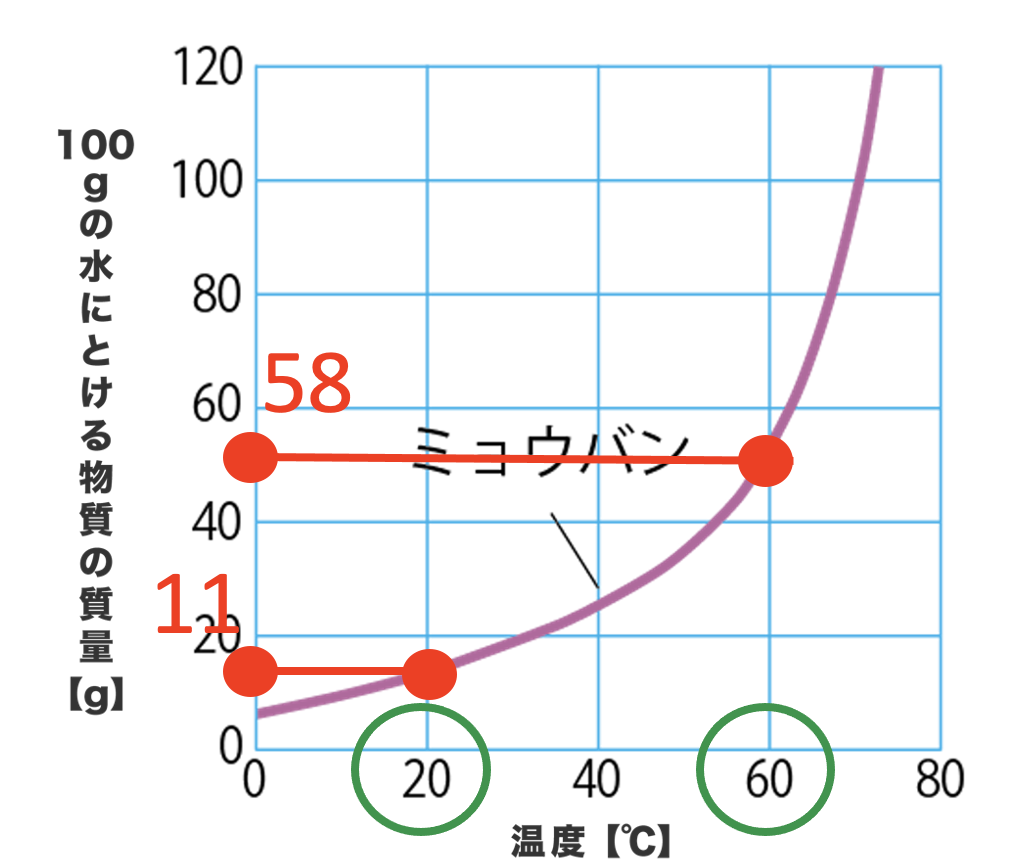

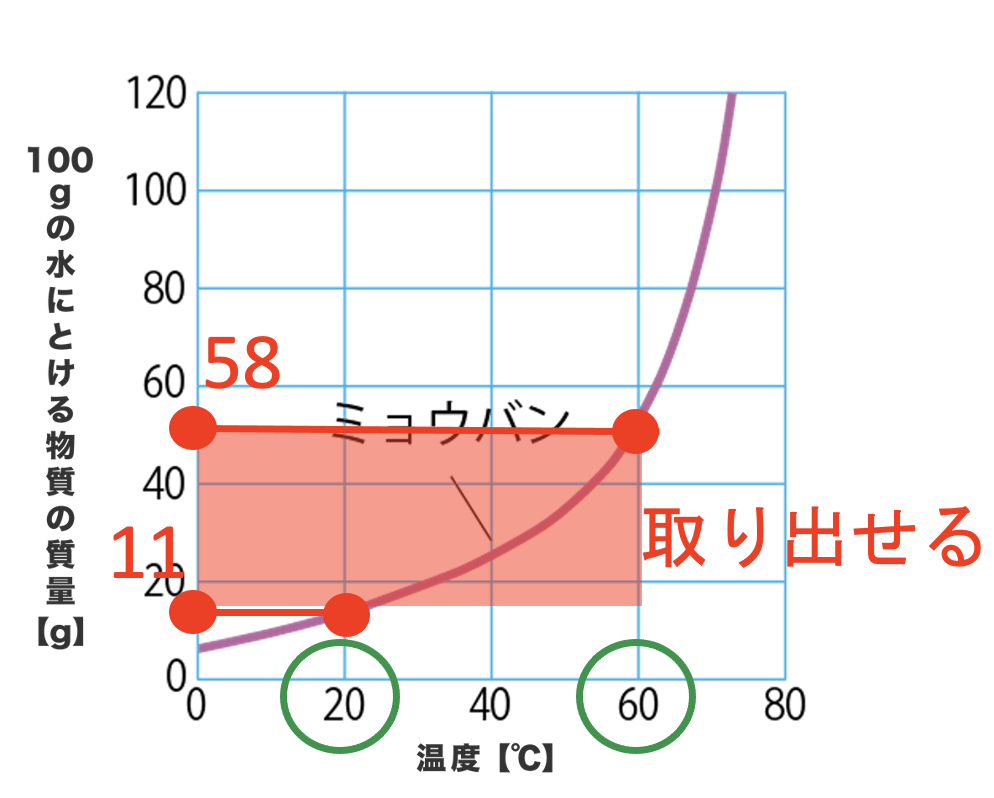
60℃では58gも溶けていたミョウバンが、20℃では11gしか溶けることができない。
つまり、58-11の47gが溶けきれず結晶として出てきてしまうんだ。
これが再結晶だよ。



人間で考えると、定員58人のバスが急に定員11人になったら、47人はバスを降りないといけないもんね。それと同じだね。
そういうことだね。これが再結晶だよ。
最後にもう一度、再結晶の言葉の意味を確認しよう。
再結晶 ⋯ 液体に溶けた物質を、再び結晶としてとりだすこと



再結晶には、溶解度の変化を利用すると良いんだね!
再結晶で取り出しにくい物質はどうするか
最後におまけで、もう少し話をするね。
再結晶で物質を取り出す際、ミョウバンのように温度による溶解度の変化が大きい物質ほど取り出しやすいんだ。

反対に下のグラフの塩化ナトリウム(食塩)をみてごらん。
温度によって溶解度がほとんど変化しないね!
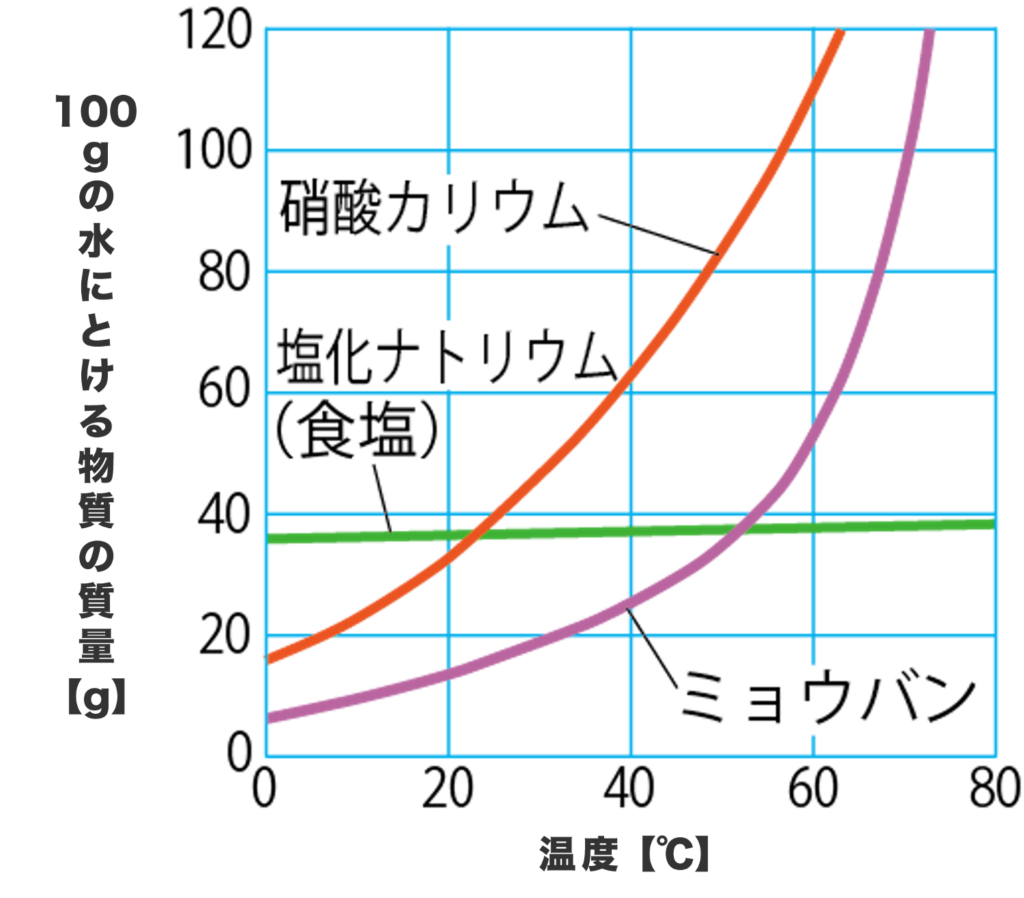




温度が変化しても、ほとんど溶解度(縦軸)が変化していないもんね⋯。
このような場合は、温度変化でたくさんの結晶を得ることが難しいから、水を蒸発させてしまって結晶を取り出したりするんだよ。
覚えておいてね!
まとめ
これで再結晶に関する話は終わりだよ。
再結晶に関する用語や、グラフの読み方をしっかりと確認しておいてね。
このサイトでは、中学理科に関する解説をまとめているよ。
またいつでも遊びにきてね!



またねー!












コメント