このページでは、金属のイオンへのなりやすさについての解説をしていくよ。
少し難しいところだけど、このページを見ればバッチリわかるようになるよ!
 ねこ吉
ねこ吉よろしくお願いします!
このサイトが本になりました!
わかりやすい解説・画像・動画が1冊に!



中学生・大人の学び直し・理科の先生などにオススメ!
それでは解説を始めます。
(動画でみたい人は↓)
イオンとは
まずはイオンとは何かについて簡単に復習をしておこう。
「イオンとは、原子が電気を帯びたもの」だったね!



帯びる?
うん。「原子が電気をもつ」と考えてもいいよ。
例えば、ナトリウム原子が電子を1つ失うと、Na+というプラスの電気を帯びたイオンになるんだ。


電子はマイナスの電気をもった粒子だから、電子を失うとプラスのイオンになるんだね。
下の塩素原子を見てみよう。塩素原子が電子を受け取ると、Clーというマイナスの電気を帯びたイオンになるんだよ。


このように、原子が電子を帯びた状態を「イオン」というんだね。
金属のイオンへのなりやすさ
では、金属のイオンへのなりやすさを見ていこう。
金属のイオンへのなりやすさを「イオン化傾向」というんだよ。
下の図を見てみよう。
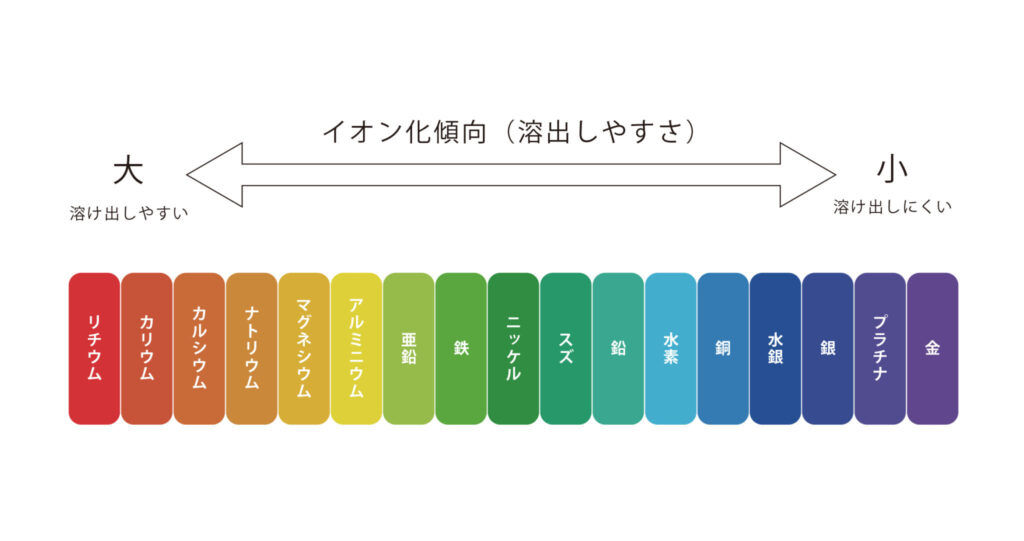

これがイオン化傾向だよ(水素は金属ではないけれど、覚えておこう)。



イオン化傾向が違うと、どのようなことが起こるの?
次の動画を見てみよう。
これは、硫酸銅水溶液に、アルミニウムを加えた動画だよ。
硫酸銅水溶液は、以下のようなイオンが含まれているよ。
陽イオン:Cu2+
陰イオン:SO42-



銅イオンが含まれているね!
その通り。「イオンになっている」とは「溶液中に溶けている」考えておくと理解しやすいかもね!
さて、動画では銅イオンが含まれる硫酸銅水溶液に、アルミニウムを加えていたね。
イオン化傾向を見てみると、銅よりもアルミニウムのほうがイオンになりやすかったよね。


つまりどのような変化が起きると考えられるかな?



イオンになりやすいアルミニウムがイオンになり、銅イオンは金属の銅になるんだね。
その通り。先ほどの動画では、そのような変化が起きていたんだね。
だからアルミニウムの周りに赤褐色の銅がくっついていたんだね。
ちなみに、銅イオンは青色をしているんだ。
銅イオンは銅へと変化し、どんどん減少していっているから、ビーカーの中の青色が薄くなっていることも見てとれるね。
もう一度、同じ動画を載せておくね。
これが、イオン化傾向による化学反応だよ。
金属のイオンのなりやすさの例題
最後に「金属のイオンのなりやすさ」の例題を考えて終わりにしよう。



問題?難しそう…。
イオン化傾向つかって考えれば簡単だよ。
では問題を見てみよう。
問題
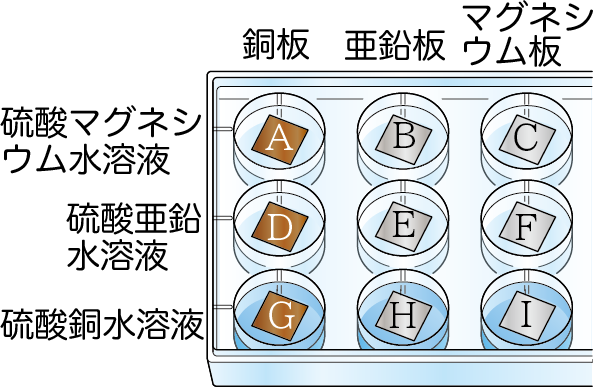
以下の水溶液に、銅板亜鉛板、マグネシウム板を加えた。


溶液や金属に変化があるのは、A~Iのどれか。
答え(タップで表示)
F・H・I
イオン化傾向をもとに考えるといいね。


マグネシウム・亜鉛・銅を比べると、イオンになりやすい順は、マグネシウム>亜鉛>銅となるね。
表にすると、以下のようになるよ。
| 銅板(Cu) | 亜鉛板(Zn) | マグネシウム板(Mg) | |
| 硫酸マグネシウム水溶液(Mg2+) | 変化なし | 変化なし | |
| 硫酸亜鉛水溶液(Zn2+) | 変化なし | 変化あり (マグネシウム→マグネシウムイオン 亜鉛イオン→亜鉛) | |
| 硫酸銅水溶液(Cu2+) | 変化あり (亜鉛→亜鉛イオン 銅イオン→銅) | 変化あり (マグネシウム→マグネシウムイオン 銅イオン→銅) |
まとめ
これで「金属のイオンのなりやすさ」の解説を終わるよ。
イオン化傾向をしっかりと覚えて、問題を解けるようにしてね!
このサイトは、中学理科に関する内容をまとめているよ。またいつでも遊びにきてね!



またねー!











コメント